스티븐스-존슨 증후군, 독성표피괴사용해
스티븐스-존슨 증후군(Stevens-Johnson Syndrome, SJS)과 독성표피괴사용해(Toxic Epidermal Necrolysis, TEN)은 피부 반점과 함께 특징적인 피부 박리, 수포를 특징으로 하는 피부와 점막 이상으로, 체표면적을 기준으로 피부 박리가 10% 미만이면 SJS, 30% 이상이면 TEN, 피부 박리가 10-30%인 경우 SJS/TEN 중첩반응(overlap SJS/TEN)으로 구분합니다.
역학
전세계적으로 TEN의 발생률은 낮으며, 매년 백만 명당 2-13명 정도 발생하는 것으로 추정됩니다.1, 2 한국인에서의 SJS과 TEN 발생률은 각각 백만 명당 3.96-5.03명, TEN의 경우 0.94-1.45명으로 낮으며, 약물에 따라 SJS/TEN 발생 비율에 차이가 있다고 알려져 있습니다.3
사망률의 경우 SJS 10%, TEN 25-35%로 추정되는데, RegiSCAR 연구자료에 따르면 6개월 내 사망 환자는 23%이며, 1년 내 사망 환자가 34%로 증가하는 것으로 나타났습니다.4 최근 KoSCAR가 주도한 한국인을 대상으로 한 연구에서 SJS/TEN의 사망률은 8.9%로 이전 연구보다는 낮았으나 여전히 높은 사망률을 보였습니다. 사망은 대부분(90%) 질병이 발생한 지 2달 이내에 발생하였으며, 회복한다고 하더라도 후유증 이환율이 높게 나타났습니다.3
전세계적으로 TEN의 발생률은 낮으며, 매년 백만 명당 2-13명 정도 발생하는 것으로 추정됩니다.1, 2 한국인에서의 SJS과 TEN 발생률은 각각 백만 명당 3.96-5.03명, TEN의 경우 0.94-1.45명으로 낮으며, 약물에 따라 SJS/TEN 발생 비율에 차이가 있다고 알려져 있습니다.3
사망률의 경우 SJS 10%, TEN 25-35%로 추정되는데, RegiSCAR 연구자료에 따르면 6개월 내 사망 환자는 23%이며, 1년 내 사망 환자가 34%로 증가하는 것으로 나타났습니다.4 최근 KoSCAR가 주도한 한국인을 대상으로 한 연구에서 SJS/TEN의 사망률은 8.9%로 이전 연구보다는 낮았으나 여전히 높은 사망률을 보였습니다. 사망은 대부분(90%) 질병이 발생한 지 2달 이내에 발생하였으며, 회복한다고 하더라도 후유증 이환율이 높게 나타났습니다.3
원인
SJS/TEN은 대부분의 경우에 약제에 의해 발생합니다. 대규모 후향적 코호트 연구에서 SJS/TEN의 원인을 살펴보았더니 89.7%가 특정 약물에 의해, 3.4%는 감염에 의해 발생하였고, 6.9%에서는 원인을 알 수 없었습니다.2, 5 원인 약물로는 알로퓨리놀(allopurinol, 13.3%), 카바마제핀(carbamazepine, 7.3%), 아목시실린(amoxicillin, 4.9%), 라모트리진(lamotrigine, 3.9%), 세파클러(cefaclor, 3.4%)가 흔하게 나타났고, 발프로에이트(valproic acid), 페니토인(phenytoin)과 같은 항경련제, 항결핵제, Trimethoprim/Sulfamethoxazole과 기타 설파계 항생제, 베타락탐 항생제, 퀴놀론계 항생제), 항염증제(특히 옥시캄 계열), 탄산탈수효소억제제 등도 SJS/TEN을 유발할 수 있습니다.2, 3
SJS/TEN은 대부분의 경우에 약제에 의해 발생합니다. 대규모 후향적 코호트 연구에서 SJS/TEN의 원인을 살펴보았더니 89.7%가 특정 약물에 의해, 3.4%는 감염에 의해 발생하였고, 6.9%에서는 원인을 알 수 없었습니다.2, 5 원인 약물로는 알로퓨리놀(allopurinol, 13.3%), 카바마제핀(carbamazepine, 7.3%), 아목시실린(amoxicillin, 4.9%), 라모트리진(lamotrigine, 3.9%), 세파클러(cefaclor, 3.4%)가 흔하게 나타났고, 발프로에이트(valproic acid), 페니토인(phenytoin)과 같은 항경련제, 항결핵제, Trimethoprim/Sulfamethoxazole과 기타 설파계 항생제, 베타락탐 항생제, 퀴놀론계 항생제), 항염증제(특히 옥시캄 계열), 탄산탈수효소억제제 등도 SJS/TEN을 유발할 수 있습니다.2, 3
잠복기
일반적으로 의심 약물을 복용한 뒤 1~3주 사이에 증상이 나타납니다.3 약물을 복용하고 8주 이후에 SJS/TEN이 발생할 가능성은 거의 없습니다.2
일반적으로 의심 약물을 복용한 뒤 1~3주 사이에 증상이 나타납니다.3 약물을 복용하고 8주 이후에 SJS/TEN이 발생할 가능성은 거의 없습니다.2
위험인자
SJS/TEN은 모든 연령층에서 발생할 수 있으며, 여성, HIV 감염자, 노인에서 좀더 많이 나타납니다. HIV 감염과 같은 면역 시스템 조절장애가 있거나, 전신 홍반 루푸스와 같은 자가면역 질환이 있거나, 악성 종양이 진행하고 있는 경우 SJS/TEN 발생 위험이 높습니다.2
SJS/TEN 발생의 유전적 소인은 특정 인간 백혈구 항원(human leukocyte antigen, HLA) 유형을 통해 예측될 수 있습니다. 대표적으로 HLA-B*58:01은 알로퓨리놀에 의한 SJS/TEN과 연관되어 있고, HLA-B*15:02는 카바마제핀에 의한 SJS/TEN의 위험지표로 알려져 있습니다. 그러나 HLA-B*15:02는 한국인에서 유전자 빈도가 0.21-0.32%로 매우 낮기 때문에 위험지표로 효용성이 없었습니다.6 이처럼 특정한 유전자와 약물 간의 연관성이 각 인종 그룹에 따라 밀접하게 영향을 받는 것이 이미 알려져 있습니다. SJS/TEN을 예측하기 위한 유전적 요소들에 대해서는 현재 진행 중인 연구 분야로 앞으로 계속적인 관심과 연구가 필요합니다. 또한, 유전적 소인뿐만 아니라 시토크롬 P450 다형성, 약물 청소율의 감소 등도 SJS/TEN 발생 위험을 높이는 데에 역할을 하는 것으로 생각됩니다.2
SJS/TEN은 모든 연령층에서 발생할 수 있으며, 여성, HIV 감염자, 노인에서 좀더 많이 나타납니다. HIV 감염과 같은 면역 시스템 조절장애가 있거나, 전신 홍반 루푸스와 같은 자가면역 질환이 있거나, 악성 종양이 진행하고 있는 경우 SJS/TEN 발생 위험이 높습니다.2
SJS/TEN 발생의 유전적 소인은 특정 인간 백혈구 항원(human leukocyte antigen, HLA) 유형을 통해 예측될 수 있습니다. 대표적으로 HLA-B*58:01은 알로퓨리놀에 의한 SJS/TEN과 연관되어 있고, HLA-B*15:02는 카바마제핀에 의한 SJS/TEN의 위험지표로 알려져 있습니다. 그러나 HLA-B*15:02는 한국인에서 유전자 빈도가 0.21-0.32%로 매우 낮기 때문에 위험지표로 효용성이 없었습니다.6 이처럼 특정한 유전자와 약물 간의 연관성이 각 인종 그룹에 따라 밀접하게 영향을 받는 것이 이미 알려져 있습니다. SJS/TEN을 예측하기 위한 유전적 요소들에 대해서는 현재 진행 중인 연구 분야로 앞으로 계속적인 관심과 연구가 필요합니다. 또한, 유전적 소인뿐만 아니라 시토크롬 P450 다형성, 약물 청소율의 감소 등도 SJS/TEN 발생 위험을 높이는 데에 역할을 하는 것으로 생각됩니다.2
증상
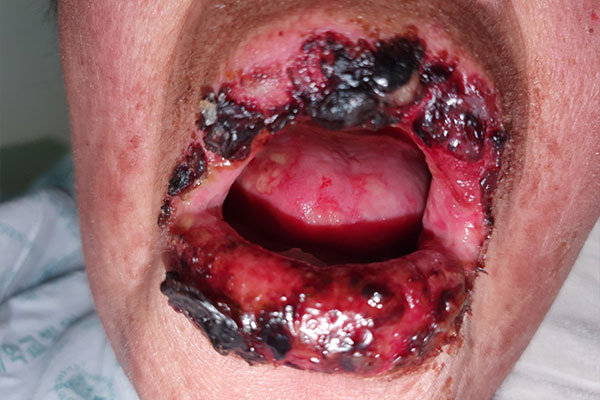
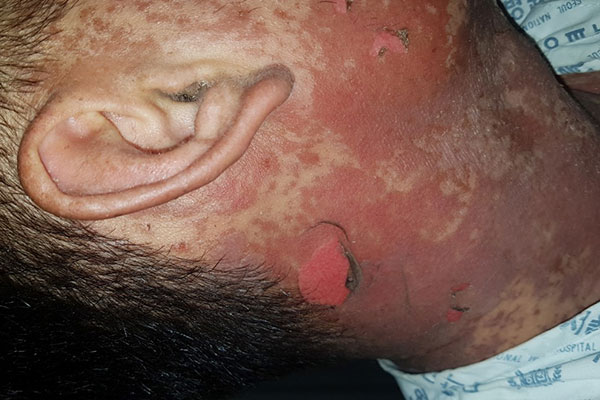
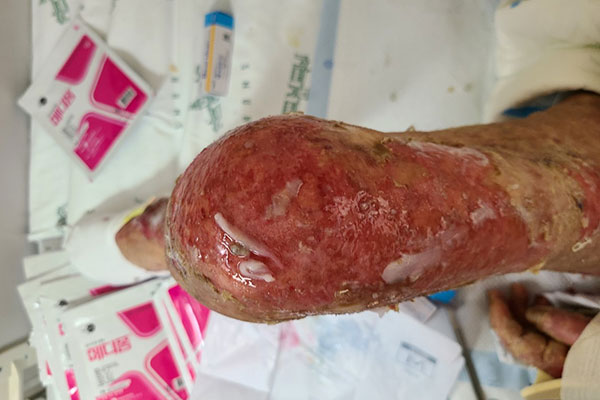
SJS/TEN의 피부 병변은 양궁 과녁처럼 다중의 고리로 이루어진 비정형 과녁형 병변(atypical target lesion)이 특징적인데, 중심부에 피부 박리에 의한 수포가 나타나며, 색깔은 짙은 편이며 자색반으로 나타나기도 합니다. 시간이 지나면서 병변이 뭉쳐지고 피부가 벗겨집니다. 피부 병변은 통증을 동반하며 주로 얼굴, 흉부에서 생겨 전신으로 퍼져 나가는 양상을 보입니다. 피부와 함께 점막도 이상소견을 보입니다. 구강점막이 흔히 침범되는데, 입술이 검붉게 보이고 통증과 출혈을 동반합니다. 안점막의 침범은 화농성 분비물을 동반하기 때문에 눈곱이 끼고 각막 궤양, 눈꺼풀염으로 진행할 수 있습니다. 후유증으로 실명을 유발할 수 있으므로 안점막 침범 여부에 주의해야 합니다. 비뇨생식기 및 호흡기 점막의 침범도 발생할 수 있습니다. 기관지를 침범할 경우 호흡곤란이 발생할 수 있습니다.7 피부 소견 외에도 발열, 혈액학적 이상(빈혈, 백혈구 감소, 혈소판 검소), 간기능 이상, 신기능 이상 등 다양한 이상 소견이 동반될 수 있습니다.
SJS, TEN의 중증도와 예후를 평가하기 위해 SCORe of TEN (SCORTEN)이라는 기준을 사용할 수 있는데, 2000년 Bastuji-Garin 등에 의해 개발되어 7가지 위험인자를 확인하여 사망률을 예측하는 것으로, 위험인자가 많을수록 사망률이 높습니다(표 1).1
SJS/TEN의 피부 병변은 양궁 과녁처럼 다중의 고리로 이루어진 비정형 과녁형 병변(atypical target lesion)이 특징적인데, 중심부에 피부 박리에 의한 수포가 나타나며, 색깔은 짙은 편이며 자색반으로 나타나기도 합니다. 시간이 지나면서 병변이 뭉쳐지고 피부가 벗겨집니다. 피부 병변은 통증을 동반하며 주로 얼굴, 흉부에서 생겨 전신으로 퍼져 나가는 양상을 보입니다. 피부와 함께 점막도 이상소견을 보입니다. 구강점막이 흔히 침범되는데, 입술이 검붉게 보이고 통증과 출혈을 동반합니다. 안점막의 침범은 화농성 분비물을 동반하기 때문에 눈곱이 끼고 각막 궤양, 눈꺼풀염으로 진행할 수 있습니다. 후유증으로 실명을 유발할 수 있으므로 안점막 침범 여부에 주의해야 합니다. 비뇨생식기 및 호흡기 점막의 침범도 발생할 수 있습니다. 기관지를 침범할 경우 호흡곤란이 발생할 수 있습니다.7 피부 소견 외에도 발열, 혈액학적 이상(빈혈, 백혈구 감소, 혈소판 검소), 간기능 이상, 신기능 이상 등 다양한 이상 소견이 동반될 수 있습니다.
SJS, TEN의 중증도와 예후를 평가하기 위해 SCORe of TEN (SCORTEN)이라는 기준을 사용할 수 있는데, 2000년 Bastuji-Garin 등에 의해 개발되어 7가지 위험인자를 확인하여 사망률을 예측하는 것으로, 위험인자가 많을수록 사망률이 높습니다(표 1).1
| Risk factors present | Mortality rate (%) |
|---|---|
| 0 - 1 2 3 4 ≥ 5 | 3 12 35 58 90 |
| The presence or absence of seven risk factors is used to determine the SCORTEN: (1) age > 40 years, (2) malignancy, (3) total body surface area affected > 10%, (4) heart rate > 120 beats per minute, (5) blood urea nitrogen > 28 mg/dL, (6) serum glucose > 250 mg/dL, (7) serum bicarbonate < 20 mEq/L. The absence of a risk factor is scored as zero; the presence of a risk factor is scored as one. SCORTEN ranges from zero to seven. | |
진단
SJS/TEN의 확진은 피부 조직검사를 통해서 이루어집니다. 특징적인 병리학적 소견은 피부 전층에 걸친 표피 괴사입니다. SJS/TEN은 중증 급성 피부 홍반 루푸스, 포도상구균 열상피부증후군, 자가면역 수포성 질환, 급성 이식편대숙주병과의 감별진단이 필요합니다. 그러나 조직학적 확진이 이루어지지 않더라도, 임상적으로 SJS/TEN과 일치하는 경우 지체하지 않고 적절한 치료를 시작해야 합니다.2
SJS/TEN의 확진은 피부 조직검사를 통해서 이루어집니다. 특징적인 병리학적 소견은 피부 전층에 걸친 표피 괴사입니다. SJS/TEN은 중증 급성 피부 홍반 루푸스, 포도상구균 열상피부증후군, 자가면역 수포성 질환, 급성 이식편대숙주병과의 감별진단이 필요합니다. 그러나 조직학적 확진이 이루어지지 않더라도, 임상적으로 SJS/TEN과 일치하는 경우 지체하지 않고 적절한 치료를 시작해야 합니다.2
치료
자세한 병력 청취를 바탕으로 원인으로 의심되는 약제를 즉시 중단하는 것이 가장 중요합니다. 피부 박리가 광범위한 경우 중환자실이나 화상치료실에서 화상환자에 준한 장기 입원치료를 해야 하며, 피부손상에 따른 수분, 전해질 및 각종 영양소 손실에 대한 적극적인 교정이 필요합니다. 감염이 의심될 경우 항생제 사용이 필요한데, 피부손상이 넓을 경우 대부분 패혈증이 발생하므로 광범위 항생제 투여를 필요로 합니다. 원인 약물 투여를 중단하더라도 면역반응은 장기간 지속될 수 있어 부신피질 스테로이드, 면역억제제 사용을 통한 면역반응 억제를 고려할 수 있습니다.
피부 병변에 대한 적절한 상처 치료가 중요하며, 안과 진료를 통해 시력저하 또는 실명의 심각한 합병증을 예방해야 합니다.
자세한 병력 청취를 바탕으로 원인으로 의심되는 약제를 즉시 중단하는 것이 가장 중요합니다. 피부 박리가 광범위한 경우 중환자실이나 화상치료실에서 화상환자에 준한 장기 입원치료를 해야 하며, 피부손상에 따른 수분, 전해질 및 각종 영양소 손실에 대한 적극적인 교정이 필요합니다. 감염이 의심될 경우 항생제 사용이 필요한데, 피부손상이 넓을 경우 대부분 패혈증이 발생하므로 광범위 항생제 투여를 필요로 합니다. 원인 약물 투여를 중단하더라도 면역반응은 장기간 지속될 수 있어 부신피질 스테로이드, 면역억제제 사용을 통한 면역반응 억제를 고려할 수 있습니다.
피부 병변에 대한 적절한 상처 치료가 중요하며, 안과 진료를 통해 시력저하 또는 실명의 심각한 합병증을 예방해야 합니다.
합병증
표피가 박리됨에 따라 탈수, 감염(패혈증), 안과적 문제, 호흡부전, 영구적인 피부 손상 등이 생길 수 있으며, 심할 경우 사망에 이를 수 있습니다. SJS/TEN 환자의 65%는 생존 이후에 눈 결막 협착, 각막 손상으로 인한 시력 저하, 회음부 협착, 모세기관지염, 탈모 등 장기간 심각한 후유증을 겪는 것으로 나타났으며, 정신적으로는 외상 후 스트레스 장애를 겪기도 합니다.
표피가 박리됨에 따라 탈수, 감염(패혈증), 안과적 문제, 호흡부전, 영구적인 피부 손상 등이 생길 수 있으며, 심할 경우 사망에 이를 수 있습니다. SJS/TEN 환자의 65%는 생존 이후에 눈 결막 협착, 각막 손상으로 인한 시력 저하, 회음부 협착, 모세기관지염, 탈모 등 장기간 심각한 후유증을 겪는 것으로 나타났으며, 정신적으로는 외상 후 스트레스 장애를 겪기도 합니다.
참고문헌
- Schneider JA, Cohen PR. Stevens-Johnson Syndrome and Toxic Epidermal Necrolysis: A Concise Review with a Comprehensive Summary of Therapeutic Interventions Emphasizing Supportive Measures. Adv Ther 2017; 34(6): 1235-44.
- Noe MH, Micheletti RG. Diagnosis and management of Stevens-Johnson syndrome/toxic epidermal necrolysis. Clin Dermatol 2020; 38(6): 607-12.
- Kang DY, Yun J, Lee SY, et al. A Nationwide Study of Severe Cutaneous Adverse Reactions Based on the Multicenter Registry in Korea. J Allergy Clin Immunol Pract 2020.
- Lee HY, Chung WH. Toxic epidermal necrolysis: the year in review. Curr Opin Allergy Clin Immunol 2013; 13(4): 330-6.
- Micheletti RG, Chiesa-Fuxench Z, Noe MH, et al. Stevens-Johnson Syndrome/Toxic Epidermal Necrolysis: A Multicenter Retrospective Study of 377 Adult Patients from the United States. J Invest Dermatol 2018; 138(11): 2315-21.
- Kim SH, Lee KW, Song WJ, et al. Carbamazepine-induced severe cutaneous adverse reactions and HLA genotypes in Koreans. Epilepsy Res 2011; 97(1-2): 190-7.
- Yang MS, Kang MG, Jung JW, et al. Clinical features and prognostic factors in severe cutaneous drug reactions. Int Arch Allergy Immunol 2013; 162(4): 346-54.

